[ad#ad4]
◆血糖値は平均と食後が大切
血糖値が健康に関係していることは周知の事実であるとおもいます。血糖値は平均的な値と食後の値が重要であることが示唆されています(1)。論文では以下のように記されています(句読点を改編しています)。
DCCTの網膜症二次予防(進展予防)における初期の数年での強化療法群における網膜症の早期進展や、Action to Control Cardiovascular Risk in Diabetes(ACCORD)試験における強化療法群での死亡率の増加は、糖尿病に伴う合併症が単なる平均血糖値の高さだけでは説明できないことを示している。
平均血糖値と独立した合併症進展の要因として考えられているのが血糖変動の大きさであり、これは低血糖と食後高血糖とに分離して考えることができる。(中略)
確定的ではないものの、一般には食後高血糖は有害であり、是正すべきであると結論してよいと思われる。
◆血糖値が高いと死亡リスクが高まる
空腹時血糖値と食後血糖値を用いて、総死亡を比較した報告があります(2)。結果は以下のようになりました。
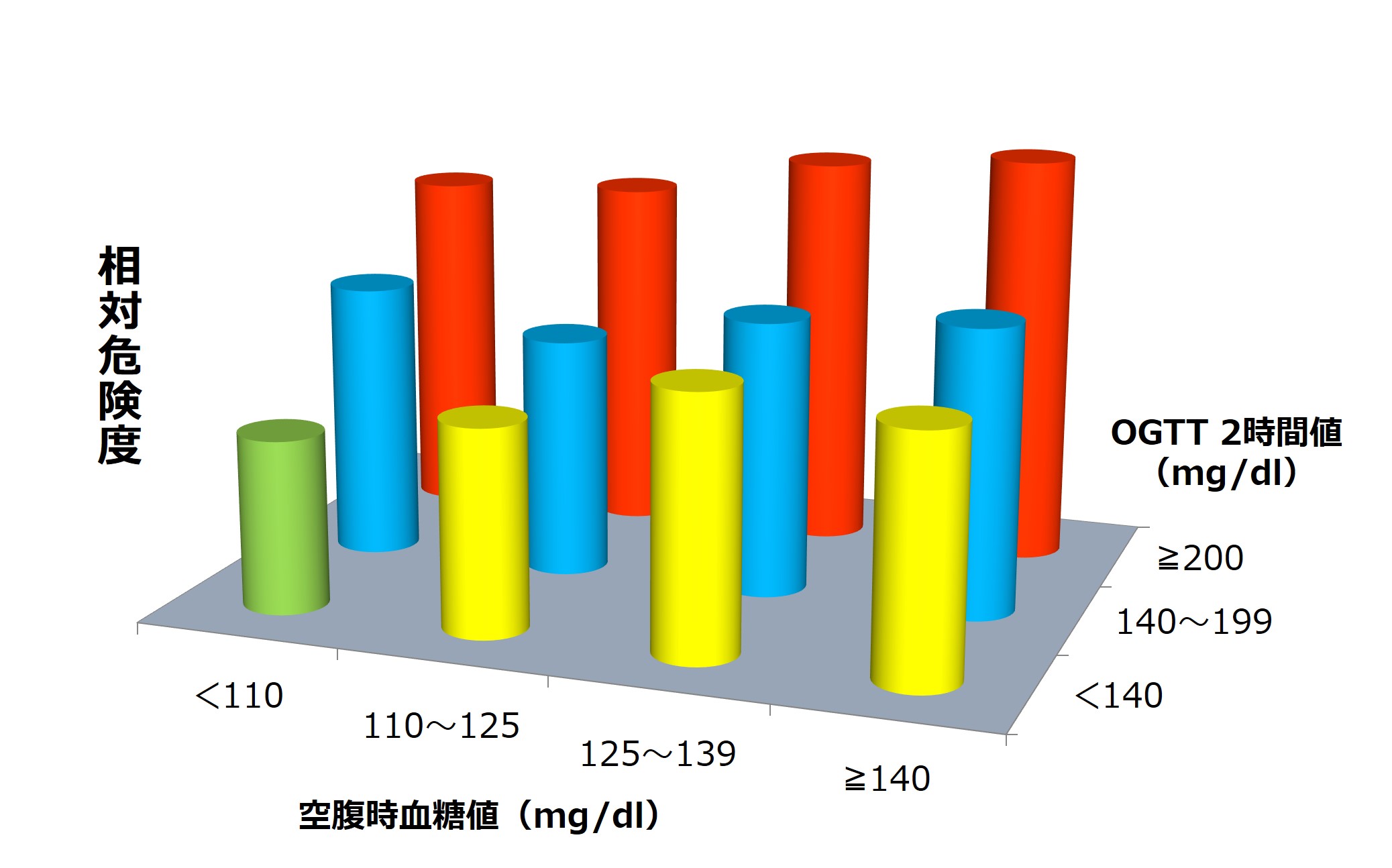
資料(2)より作成
空腹(平均)時と食後の血糖値が高いほど、おおむね総死亡の相対危険度が高い傾向にありました。やはり、空腹時(平均)血糖値と食後血糖値の両方を気にかけたほうがよさそうです。
◆食事だけでは改善しない!?
昨今では、糖質制限食など食事療法をよく目にしますね。
しかし、肥満者・肥満糖尿病患者を対象にした研究によると、食事療法(食事制限)だけでは内臓脂肪は減少せず、LBM(除脂肪体重)が減少、インスリン抵抗性は改善しなかったとのこと(3)。
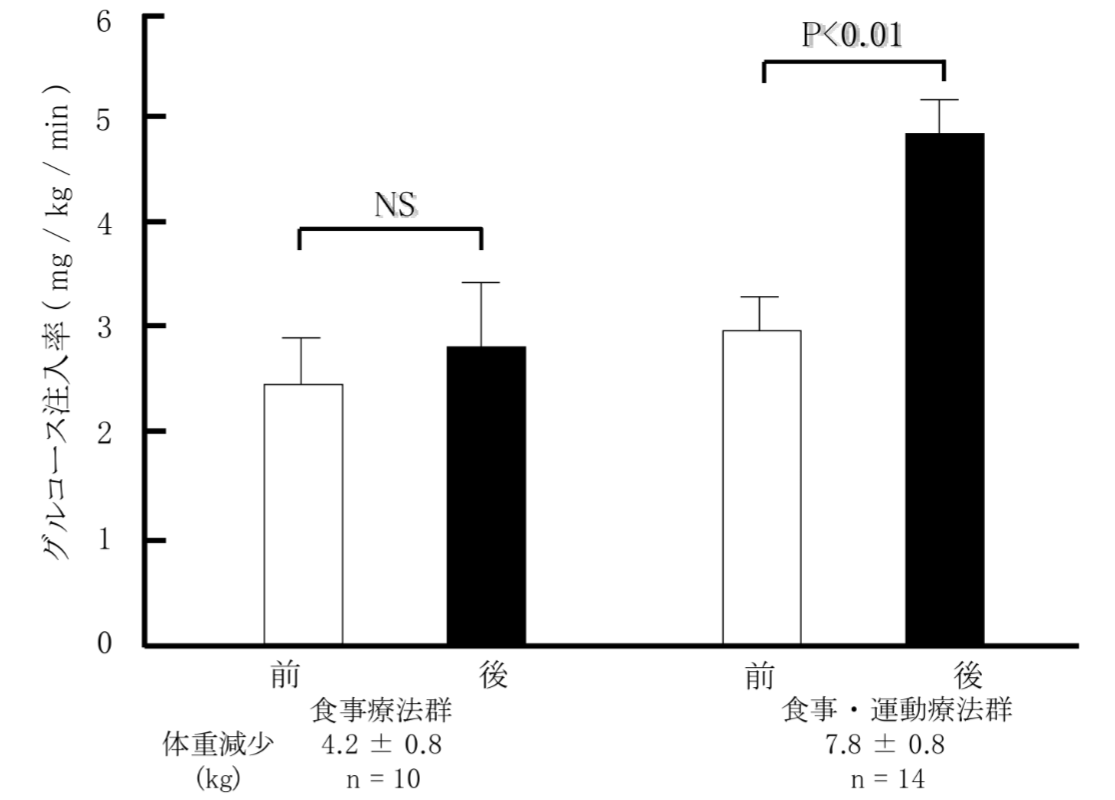
資料(3)より引用、原典(4)
この報告は対象者が少なく、個人的には減量には食事のほうが関わってると思うので鵜呑みにはできません。しかし、間接的に運動療法が重要であるというのはあるだろうと思われます。
さて、血糖を是正するために、運動療法にはどのくらい効果があるのでしょうか?すこし調べてみることにしました。
[ad#ad7]
◆運動療法のエビデンス
1.NEAT(運動以外の身体活動量)
Umpierreらのメタアナリシスによると、HbA1c(平均血糖値)の低下には、運動量(頻度)の増加と相関があり、運動強度とは相関がなかったとのこと(5)。
つまり、運動のきつさよりも運動の時間のほうがHbA1c改善にはよいかもしれないということです。
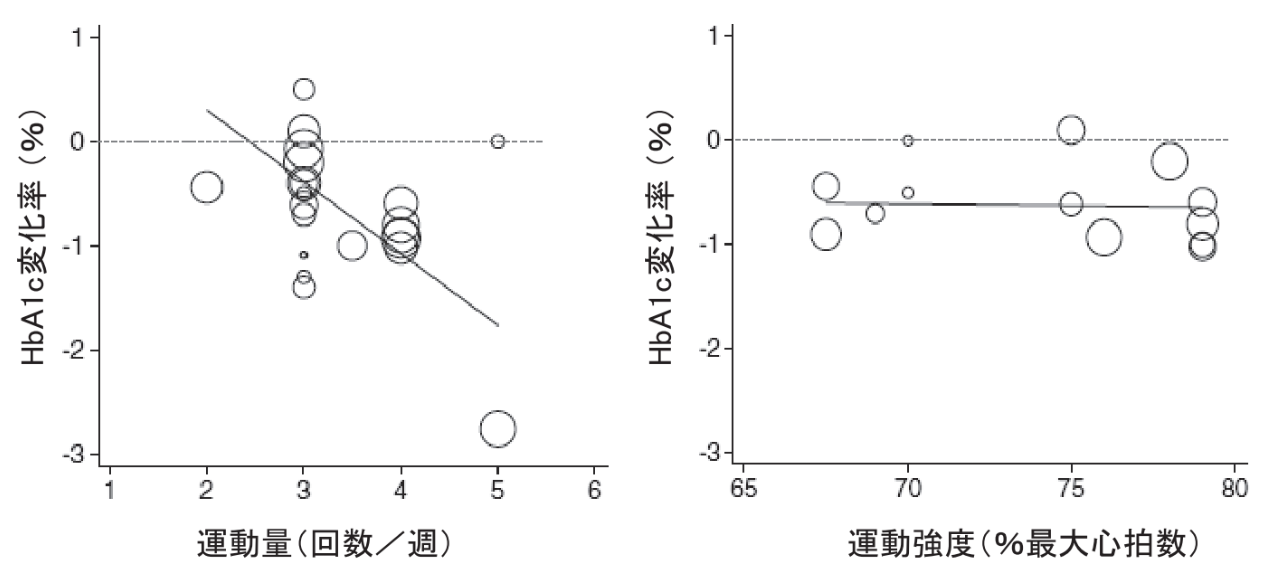
資料(6)より引用、原典(5)
最近はNEATというものが重要であることがいわれています。NEATというのは、non-exercise activity thermogenesisの略で、「運動以外の身体活動」のことを指しています。
以前、座位時間といった身体不活動時間が増えると、死亡リスクや糖尿病リスクが高まることを書きました(参照:座りすぎが病を生む!座りすぎのリスクと対策について)。
Ploegらの心疾患既往者・糖尿病患者を対象にした報告によれば、座位時間が長いと、歩行時間が長くても死亡数が変わりませんでした(7)。つまり、座位によって、歩行の効果が相殺されてしまったということです。
いくら十分な運動をしていても、それ以外の活動量(NEAT)が少ないと、死亡リスクが高くなる可能性があります。食事や運動も大切ですが、そのベースにはNEATが欠かせません。なるべく小まめに動くことを心がけましょう。
2.筋力トレーニング
(1)筋肉減少と高血糖
肥満女性を対象にした研究によれば、インスリン抵抗性の改善には、骨格筋量が重要であることが示唆されています(8)。
また、今年(2018年)になってでた報告に、痩せている閉経女性のなかでどのような人が高血糖になりやすいかを調査したものがあります(9)。
それによると、インスリンの分泌が低いことにくわえて、LBM(除脂肪体重)が少ない人、細胞内に脂肪(異所性脂肪)が蓄積している人ほど、血糖値が高いことが明らかになりました。
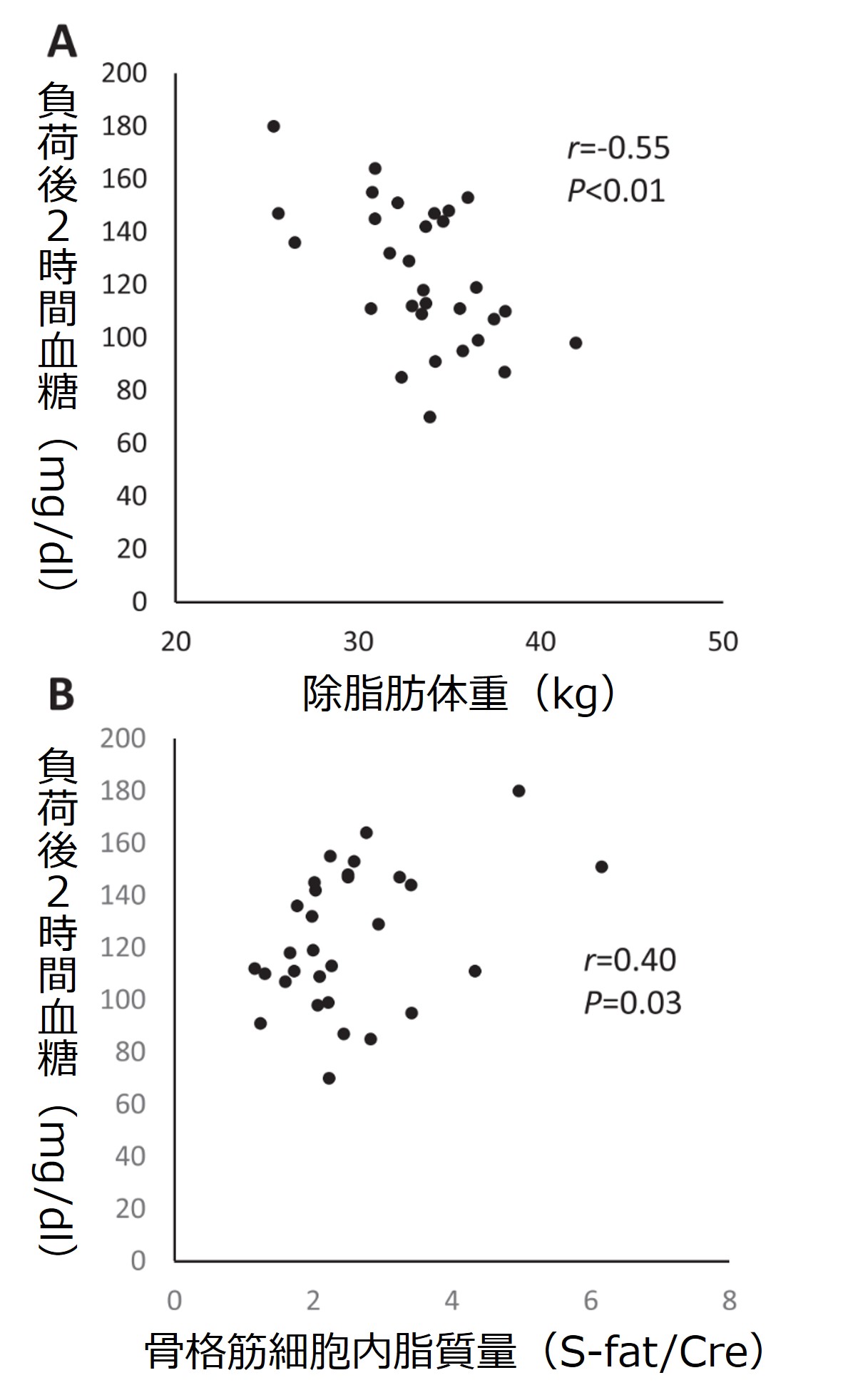
資料(9)より引用改編
つまり、筋肉量が少なく、脂肪が多い、いわゆるサルコペニア肥満の女性が高血糖になりやすかったということですね。
ちなみにサルコペニア肥満は、単独の筋肉減少(サルコペニア)や脂肪増加(肥満)よりも死亡率などが高くなるので注意が必要です(10)。
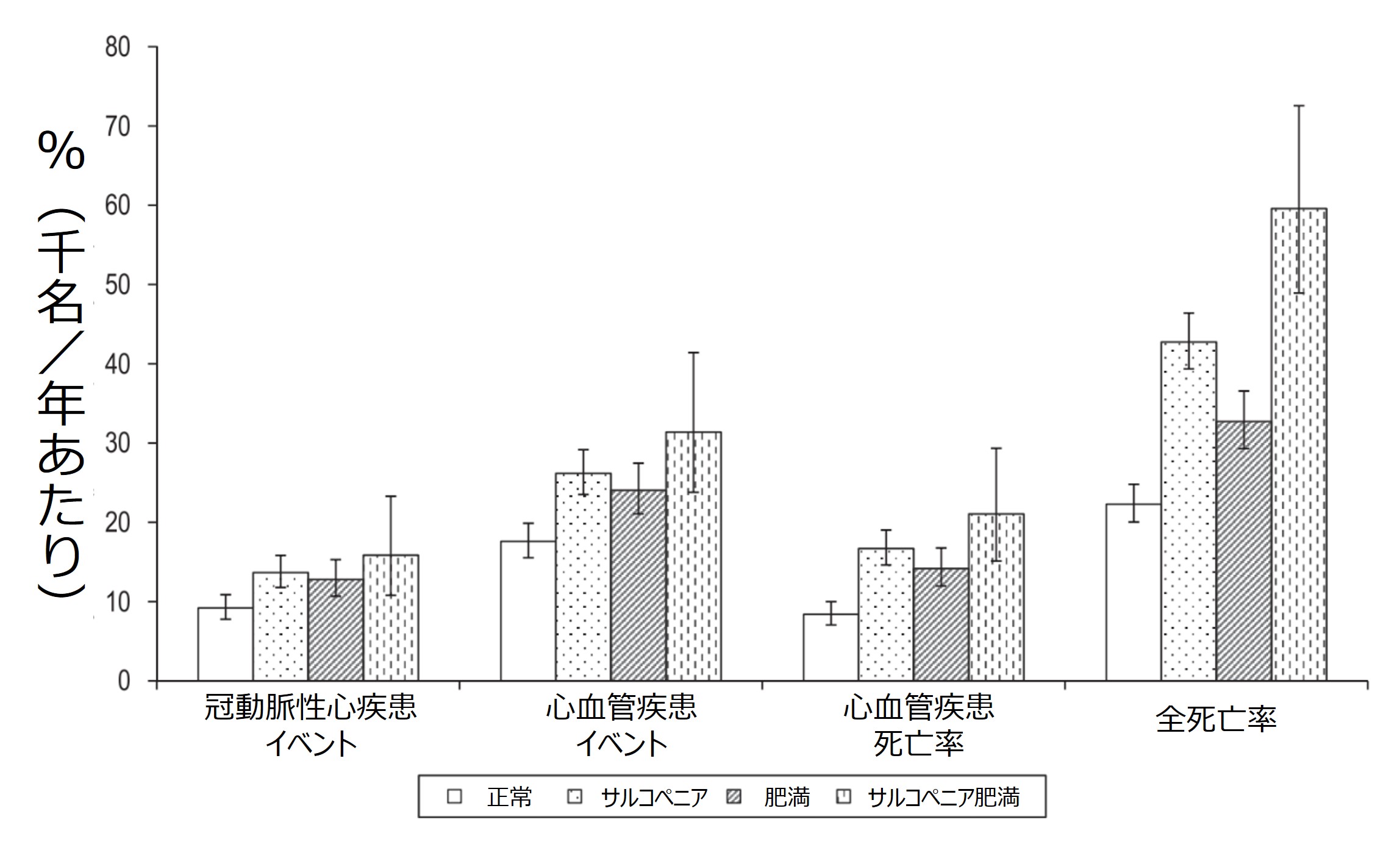
資料(10)より引用改編
(2)運動による血糖低下のメカニズム
さきに結論を言っておくと、筋トレは血糖値を下げる効果があるようです。その理由を理解するためには、運動による血糖低下のメカニズムを知っておく必要があります。
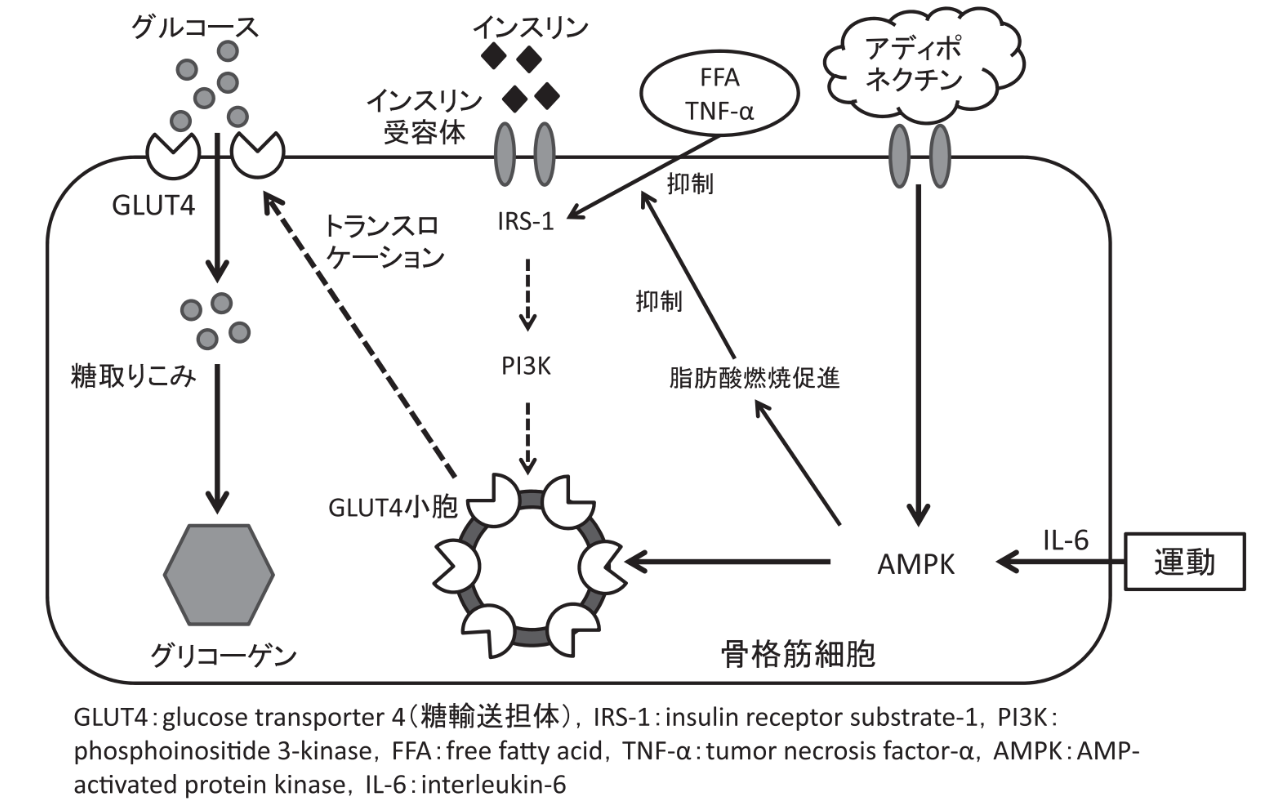
資料(6)より引用
通常は糖分(グルコース)が身体に入ってくると、それを細胞内に取り込むためにインスリンが分泌されます。インスリンはインスリン受容体に接合します。そしていくつかのシグナルを介して糖輸送体(glucose tranceporter 4:GLUT4)へと伝わり、それが細胞膜に移動し、糖分が取り込まれることで血糖値が下がります。
では、運動の場合はどうなるか?
運動をすると骨格筋の筋収縮がおこります。すると、骨格筋のAMPキナーゼ(AMPK)が活性化し、GLUT4が筋の細胞膜へ移動してきて、糖の取り込みが促進されるので血糖値が下がります。この場合はインスリンの分泌が必要ないので、身体にも優しいですね。
体内の糖分の取り込みは、ほとんど(85%以上)が筋肉でおこなわれているといわれています。筋肉が減ると、糖分の代謝が悪くなったり行き場がなくなり、血糖値のコントロールに悪影響がでてきます。ゆえに、筋トレをして筋肉を増やすことが、耐糖能(血糖コントロール)に重要なんですね。
また、運動には以下のような働きもあり、それらが多面的に血糖値をさげることに寄与しています。
・筋肉から産生・分泌されるマイオカインのひとつであるIL-6(interleukin-6)が、AMPK活性化をかいして糖の取りこみを促進する(11)
・インクレチン分泌を促進して、インスリン分泌を増加させ、糖代謝を改善する(12)
注意としては、筋トレするタイミングですね。食後は同化モード、つまり身体を合成している状態になっているので、筋トレのような異化(分解)を促進するものとは相反するものになります。よって、筋トレは食後ではなく、食前(空腹時)におこなうのがよいかもしれません。
3.有酸素トレーニング
日本人男性約4700名を対象にしたコホート研究によれば、持久力(最大酸素摂取量)が高い人ほど2型糖尿病の罹患リスクが低い傾向にあったという報告があります(13)。
そして、そのコホート研究の経過を引きつづき解析したところ、持久力が上昇(低下→増加)した人は、糖尿病の発症率が低くなったとのこと(14)。
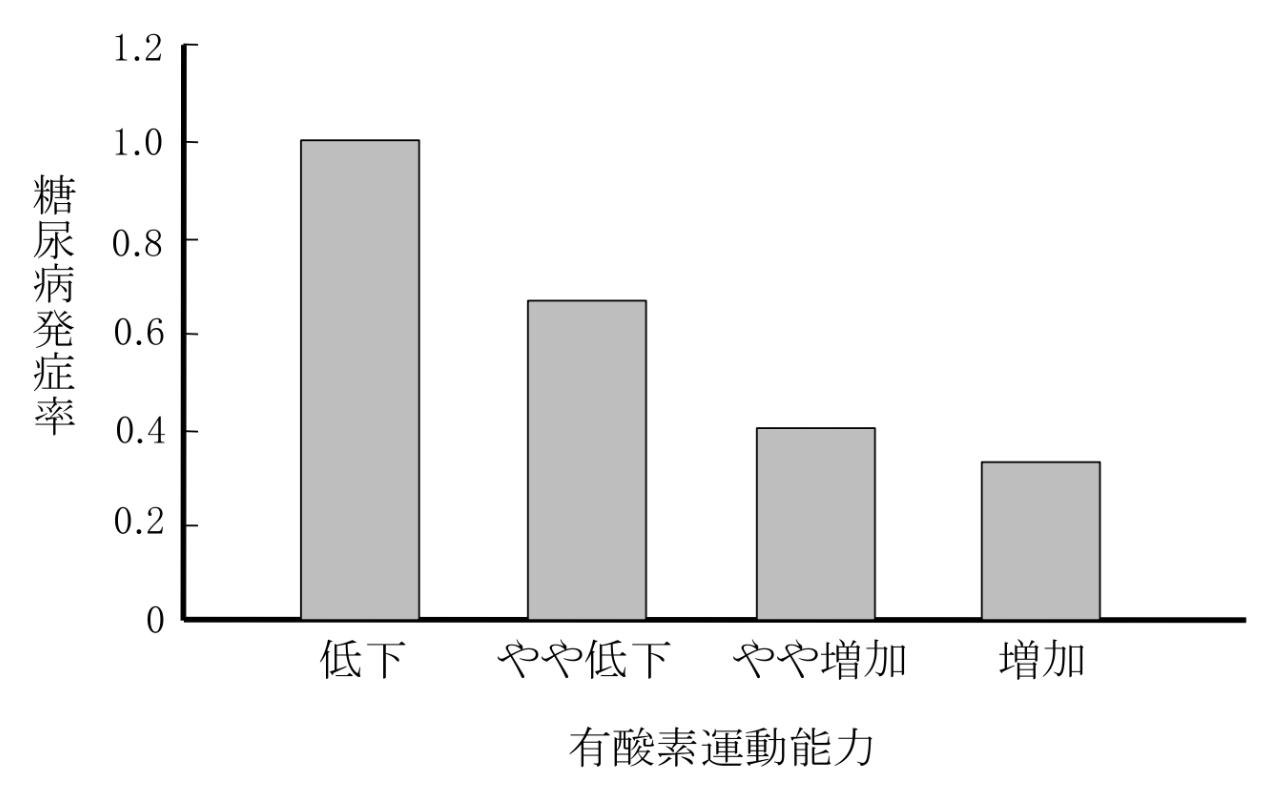
資料(3)より引用、原典(14)
持久力は耐糖能(血糖コントロール)に重要のようですね。
(1)低~中強度トレーニング
食後のウォーキングといった有酸素運動は、食後高血糖を抑えるのに有用であるということが報告されています(15.16)。このことは以前の記事でもすこし触れました(参照:ウォーキングと大気汚染~運動が逆に不健康になる!?~)。
食後はちょっと散歩したり足踏みしたり、後述するように立っているだけでもいいので、まずは横にならないようにすることがポイントです。
(2)高強度トレーニング
5~20分/回の高強度の運動によって、1~3日にわたり血糖値がコントロールされたという報告があります(17)。
これは健常者でも糖尿病患者でも変わりなかったようです。また、2型糖尿病患者にたいして2週間のプログラムをおこなったところ、運動後48時間から72時間で平均血糖値が13%低下し、GLUT4の出現が369%増加しました。
(3)有酸素運動のさまざまな方法
有酸素運動は持続的でなく、小まめにやっても血糖低下作用があるという報告があります(18)。
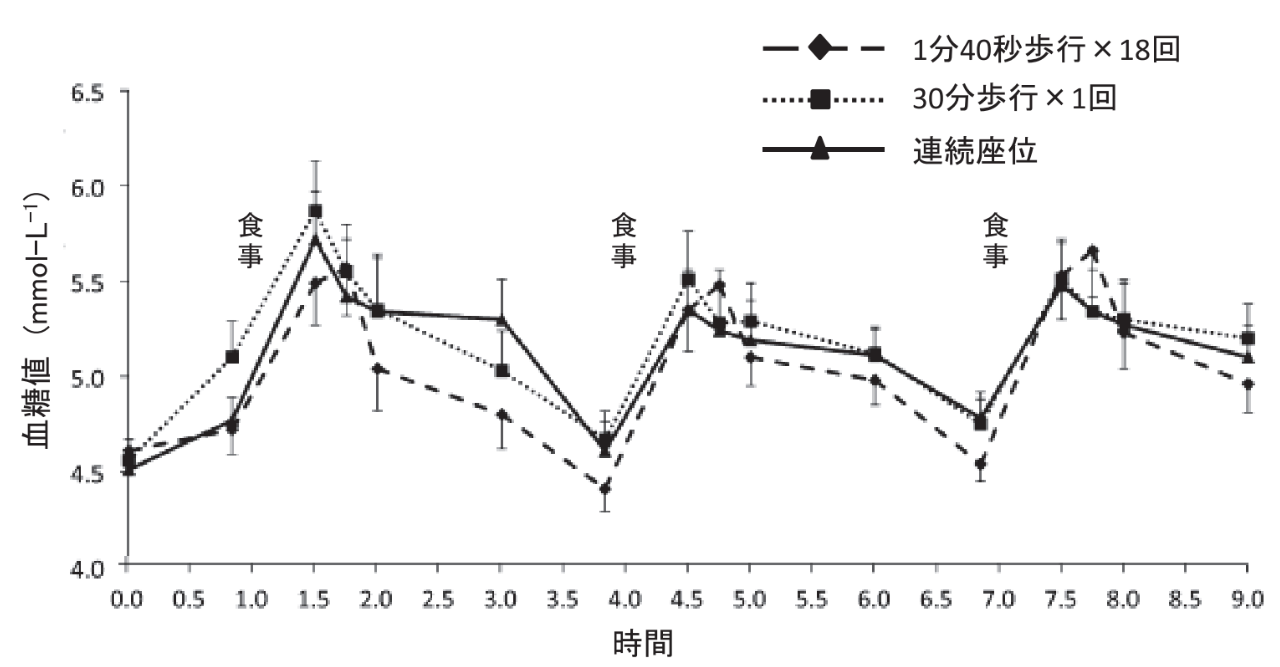
資料(6)より引用、原典(18)
研究はデスクワークの健常成人を対象にしたものです。
①1日1回30分の歩行をした場合
②30分ごとに1分40秒の歩行した場合
血糖値とインスリン値の変化を検討しました。結果は②の場合では①とくらべて、曲線下面積にて血糖値は37%、インスリン値は18%減少しました。
また、2型糖尿病ハイリスクの閉経女性を対象にした研究があります(19)。それによると、立っているだけでも歩行と同じくらいの血糖降下作用が示唆されました。インスリン値も歩行までにはおよばないものの、立っているだけで減少が認められました。
ほかにも2型糖尿病患者に、食後60分と120分に階段昇降を3分間おこなわせて血糖の変化を検討した研究があります(20)。
結果は、安静日と比較して有意に血糖値が減少しました。たった3分の階段昇降を2回おこなうだけで、耐糖能(血糖コントロール)が改善できるということですね。
立つ時間を増やす、階段を使うようにするといった小さなことから始めてみるだけでも、血糖のコントロールに効果があるかもしれません。
4.筋力と有酸素の組み合わせが効果的
2型糖尿病患者を対象にした研究によれば、単独で筋トレや有酸素トレーニングをおこなうより、両方を併用したほうが血糖を下げるのに効果があるとのことです(21)。
研究では262人をランダムに4つの群にわけました。各群は9カ月間にわたり以下のプログラムを実施しました。
①筋力トレーニング群(73人)
②有酸素トレーニング群(72人)
③併用(筋トレ+有酸素)群(76人)
④運動を行わない対照群(41人)
・筋力トレーニング群では全身の筋トレを週3回[上半身(ベンチプレス、シーテッド・ロウイング、ショルダープレス、ラットプルダウン)2セット、下半身(レッグプレス、レッグエクステンション、スクワット)3セット、腹筋・背筋運動2セット]
・有酸素トレーニング群では中等度の運動(最大酸素摂取量50~80%)を週に150分(12kcal/kg/週)
・併用群では有酸素トレーニング(10kcal/kg/週)と筋トレ(2回/週)
・対照群ではストレッチとリラクゼーション(1回/週)
結果は以下のようになりました。
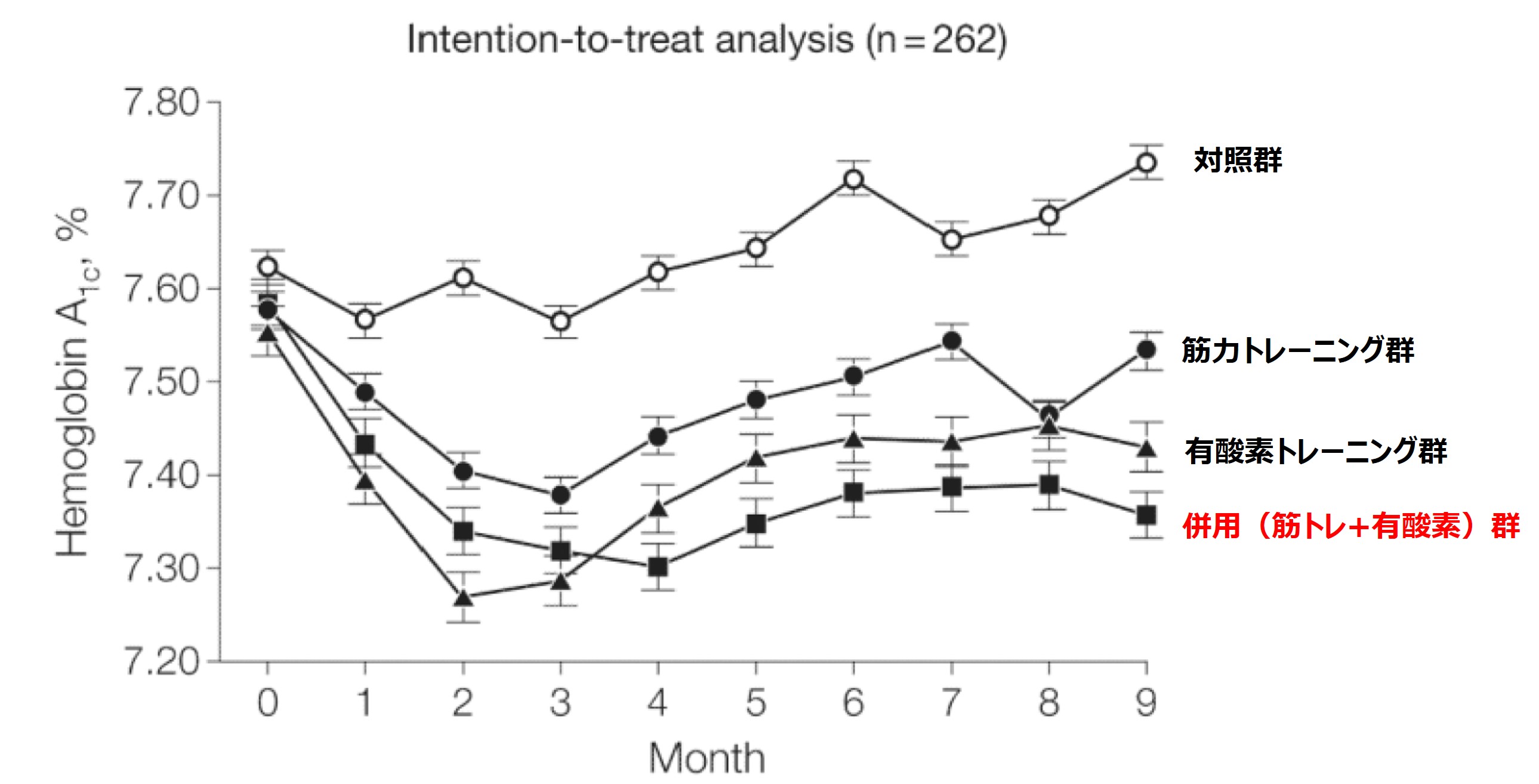
資料(20)より引用改編
対照群と比較して、併用群のみでHbA1c値が有意に低下していました。対照群との差は-0.34%(95%CI:-0.64~-0.03、p=0.03)でした。
筋力トレーニング群は-0.16%(95%CI:-0.46~0.15、p=0.32)、有酸素トレーニング群は-0.24%(95%CI:-0.55~0.07、p=0.14)と低下してはいましたが、有意差は認められませんでした。
筋トレと有酸素トレーニングは、バランスよく行ったほうがよさそうですね。ちなみに、2010年に発表された、アメリカ糖尿病学会とアメリカスポーツ医学会の共同運動指針でも、筋トレと有酸素運動をあわせておこなうことが提唱されています(22)。
◆耐糖能改善には体重減少が重要?
Rossの報告によれば、運動による耐糖能の改善は体重減少(肥満解消)がポイントであることが示唆されています(23)。
また、肥満高齢者を対象にしたRCTがあります(24)。「食事による体重減少」と「食事による体重減少+運動」の2つの群にわけて調査したものです。
それによると、インスリン感受性と肝臓内脂肪量の変化が有意に相関したとのこと。そして運動をプラスしたからといって、耐糖能改善の効果が有意に増加することはありませんでした。
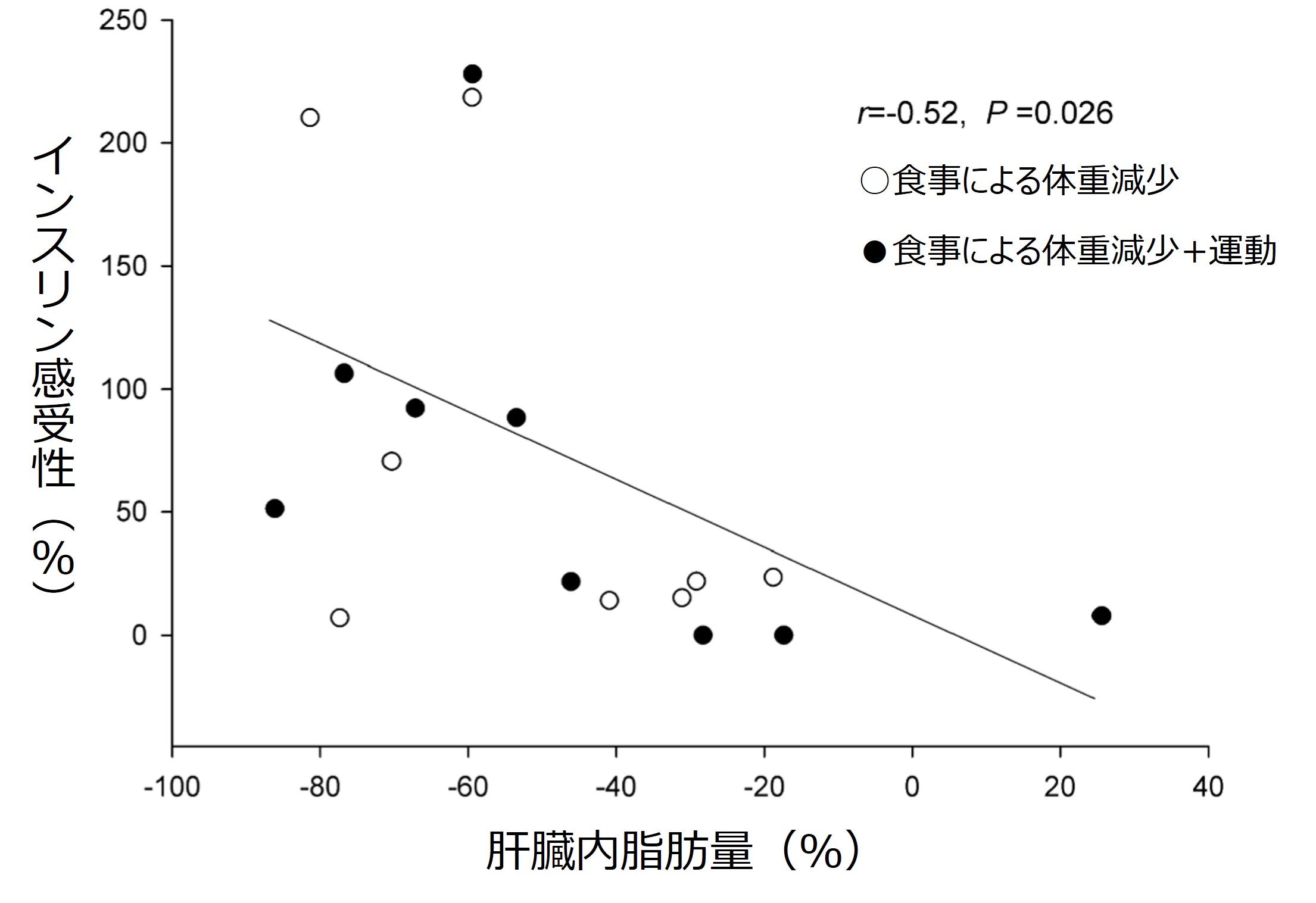
資料(24)より引用改編
つまり、耐糖能を改善するには体重減少(肥満解消)こそがポイントかもしれないということですね。これは脂肪毒性などが関与しているのかもしれません(参照:サルコペニアの原因と確認のための指輪っかテスト)。
運動は耐糖能の改善に即時効果はありますが、長期的な効果を望むのであれば、食事などによる体重管理(減量など)は欠かせないと思います。
●運動→インスリンを用いない糖取り込みの促進(即時・対症的)
●食事・運動→減量による耐糖能改善(長期・根治的)
◆まとめ
・耐糖能改善に運動は有用。
・ベースとしてNEAT(運動以外の身体活動)を増やす。
・筋トレや有酸素運動をバランスよくおこなう。
・体重管理(減量など)が重要そう。
とくに目新しいこともなく当たり前な結論ですね。いろいろ健康法はありますが、まずは基本を大切にですね。
減量などの目標を立ててもうまくいかない人は、WOOPなどを使用してみるのも一策です(参照:WOOP~科学的に認められた目標を達成するための法則~)。
【資料】
(1)山田悟、食後高血糖は有害か : 臨床的エビデンスに基づく検証 (特集 食後高血糖改善薬による糖尿病治療)、糖尿病 5(12);14-19、2013
(2)Glucose tolerance and mortality: comparison of WHO and American Diabetes Association diagnostic criteria. The DECODE study group. European Diabetes Epidemiology Group. Diabetes Epidemiology: Collaborative analysis Of Diagnostic criteria in Europe.[PMID:10466661]
(3)佐藤佑造、食習慣・運動習慣と生活習慣病:糖尿病を中心として、瀬木学園紀要 (8)、1、2014
(4)Daily walking combined with diet therapy is a useful means for obese NIDDM patients not only to reduce body weight but also to improve insulin sensitivity.[PMID:7555502]
(5)Volume of supervised exercise training impacts glycaemic control in patients with type 2 diabetes: a systematic review with meta-regression analysis.[PMID:23160642]
(6)井垣誠、糖尿病に対する運動療法の最前線、理学療法学 43(6)、508-513、2016
(7)Sitting time and all-cause mortality risk in 222 497 Australian adults.[PMID:22450936]
(8)Importance of Lean Muscle Maintenance to Improve Insulin Resistance by Body Weight Reduction in Female Patients with Obesity.[PMID:27126885]
(9)Characteristics of Glucose Metabolism in Underweight Japanese Women.[PMID:29600294]
(10)Sarcopenic obesity and risk of cardiovascular disease and mortality: a population-based cohort study of older men.[PMID:24428349]
(11)Muscles, exercise and obesity: skeletal muscle as a secretory organ.[PMID:22473333]
(12)Interleukin-6 enhances insulin secretion by increasing glucagon-like peptide-1 secretion from L cells and alpha cells.[PMID:22037645]
(13)Cardiorespiratory fitness and the incidence of type 2 diabetes: prospective study of Japanese men.[PMID:14514602]
(14)Long-term trends in cardiorespiratory fitness and the incidence of type 2 diabetes.[PMID:20215460]
(15)Advice to walk after meals is more effective for lowering postprandial glycaemia in type 2 diabetes mellitus than advice that does not specify timing: a randomised crossover study.[PMID:27747394]
(16)Exercise after You Eat: Hitting the Postprandial Glucose Target.[PMID:28974942]
(17)The impact of brief high-intensity exercise on blood glucose levels.[PMID:23467903]
(18)Breaking prolonged sitting reduces postprandial glycemia in healthy, normal-weight adults: a randomized crossover trial.[PMID:23803893]
(19)Breaking Up Prolonged Sitting With Standing or Walking Attenuates the Postprandial Metabolic Response in Postmenopausal Women: A Randomized Acute Study.[PMID:26628415]
(20)Stair climbing/descending exercise for a short time decreases blood glucose levels after a meal in people with type 2 diabetes.[PMID:27547414]
(21)Effects of aerobic and resistance training on hemoglobin A1c levels in patients with type 2 diabetes: a randomized controlled trial.[PMID:21098771]
(22)Exercise and type 2 diabetes: the American College of Sports Medicine and the American Diabetes Association: joint position statement.[PMID:21115758]
(23)Does exercise without weight loss improve insulin sensitivity?[PMID:12610063]
(24)Diet and exercise interventions reduce intrahepatic fat content and improve insulin sensitivity in obese older adults.[PMID:19390517]
[ad#ad3]